Тромботические массы: состав, причины и последствия образования
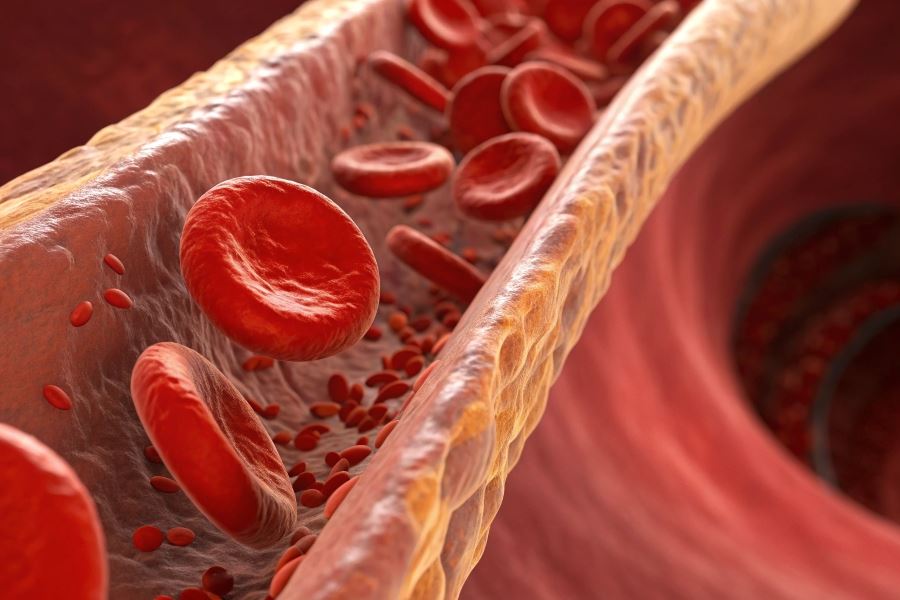
Тромботические массы представляют собой патологические образования, формирующиеся внутри кровеносных сосудов в результате нарушения нормального кровотока. По своей сути, это сгустки крови, состоящие из нескольких ключевых компонентов:
- Фибрин — нерастворимый белок, образующий основной каркас тромба. Он формируется из растворимого белка фибриногена под действием фермента тромбина и создает прочную сетчатую структуру.
- Тромбоциты (кровяные пластинки) — безъядерные клеточные фрагменты, которые первыми реагируют на повреждение сосудистой стенки, прилипая к ней и друг к другу, образуя так называемую тромбоцитарную пробку.
- Эритроциты (красные кровяные клетки) — захватываются фибриновой сетью и составляют значительную часть объема тромба, придавая ему характерный красный цвет.
- Лейкоциты — в меньшем количестве также могут присутствовать в составе тромботических масс, особенно при воспалительных процессах.
В зависимости от преобладающего компонента различают белые тромбы (богатые тромбоцитами и фибрином) и красные тромбы (с высоким содержанием эритроцитов).
Механизм образования и отличительные особенности
Формирование тромботических масс происходит в результате активации системы свертывания крови, которая в норме защищает организм от кровопотери при повреждении сосудов. Этот процесс запускается при наличии одного или нескольких факторов из классической триады Вирхова:
- Повреждение эндотелия (внутренней выстилки сосудов) — может быть вызвано травмой, воспалением, атеросклеротическими бляшками или токсическими веществами.
- Замедление кровотока (стаз) — наблюдается при длительной иммобилизации, сердечной недостаточности или варикозном расширении вен.
- Гиперкоагуляция — повышенная свертываемость крови из-за генетических особенностей, приема определенных лекарств, беременности или онкологических заболеваний.
Важно отметить, что тромботические массы формируются в живом организме в результате физиологических процессов, в отличие от посмертных сгустков крови.
Тромботические массы следует отличать от других патологических образований в сосудах:
- От атеросклеротических бляшек, которые формируются в стенке артерии и состоят преимущественно из липидов, соединительной ткани и кальцификатов.
- От эмболов — оторвавшихся и мигрирующих по кровотоку фрагментов тромбов или других материалов (жир, воздух, амниотическая жидкость).
- От вегетаций — образований на клапанах сердца при инфекционном эндокардите, состоящих из фибрина, тромбоцитов и микроорганизмов.
Тромботические массы могут быть окклюзивными (полностью перекрывающими просвет сосуда) или пристеночными (частично суживающими просвет). В зависимости от локализации и размера они могут вызывать различные клинические проявления — от бессимптомного течения до жизнеугрожающих состояний, таких как инфаркт миокарда, ишемический инсульт или тромбоэмболия легочной артерии.
Диагностика и лечение состояний, связанных с тромботическими массами
Современные методы диагностики
Диагностика тромботических масс в современной медицине основывается на комплексном подходе. Ультразвуковое исследование с допплерографией остается методом первой линии благодаря неинвазивности и доступности. Современные УЗИ-аппараты экспертного класса позволяют визуализировать тромбы размером от 2 мм с чувствительностью до 95% при исследовании периферических сосудов.
МРТ с контрастированием обеспечивает детальную визуализацию тромботических масс даже в труднодоступных областях. Технология МР-венографии позволяет создавать трехмерные реконструкции венозной системы без использования ионизирующего излучения.
КТ-ангиография с контрастированием является золотым стандартом для диагностики тромбоэмболии легочной артерии и имеет чувствительность до 97% при выявлении тромбов в крупных сосудах.
Лабораторная диагностика включает определение D-димера – продукта деградации фибрина, уровень которого повышается при активном тромбообразовании. Новые высокочувствительные тесты на D-димер имеют отрицательную прогностическую ценность до 99%, что позволяет с высокой вероятностью исключить наличие тромбоза при отрицательном результате.
Перспективным направлением является определение микроРНК (miR-126, miR-134, miR-145), которые могут служить ранними биомаркерами тромбообразования еще до появления клинических симптомов.
Современные подходы к лечению
Медикаментозная терапия остается основой лечения большинства тромботических состояний. Прямые оральные антикоагулянты (ПОАК) – ривароксабан, апиксабан, дабигатран – постепенно вытесняют варфарин благодаря предсказуемой фармакокинетике и отсутствию необходимости регулярного контроля МНО. Исследования показывают, что ПОАК снижают риск геморрагических осложнений на 30-40% по сравнению с варфарином.
Тромболитическая терапия с использованием рекомбинантного тканевого активатора плазминогена (rt-PA) эффективна при массивной тромбоэмболии легочной артерии и ишемическом инсульте в первые часы после появления симптомов. Новые тромболитики с увеличенным периодом полувыведения (тенектеплаза) позволяют проводить болюсное введение вместо длительной инфузии.
Катетер-направленный тромболизис с использованием ультразвуковых катетеров EKOS сочетает локальное введение тромболитика с механическим воздействием ультразвука, что повышает эффективность растворения тромба на 50-60% и снижает риск системных геморрагических осложнений.
Хирургические методы включают тромбэктомию, установку кава-фильтров и стентирование. Эндоваскулярная тромбэктомия с использованием стент-ретриверов стала стандартом лечения ишемического инсульта при окклюзии крупных церебральных артерий, увеличивая шансы на благоприятный исход на 30-40%.
Профилактика тромбообразования включает раннюю активизацию пациентов после операций, применение компрессионного трикотажа и медикаментозную профилактику у пациентов высокого риска. Персонализированный подход к профилактике с использованием генетического тестирования на наследственные тромбофилии позволяет выявлять пациентов с повышенным риском тромбообразования и назначать им индивидуальные схемы профилактики.
